亜鉛-マンガン電池の再発見 二次電池化と高容量化によって広がる未来
発表のポイント
- 弱酸性水溶液中におけるMnO2の析出/溶解反応を利用し、2電子移動に基づく高容量二次電池を開発
- 集電体にカーボンフェルトを採用し、Zn2+およびMn2+を含む電解液に、バッファーとFe3+を添加することで可逆性と高い面積比容量を実現
- 従来の理解を覆す新知見:立命館大学SRセンターでの放射光分析により、強酸性条件下で言われてきた放電過程でのMnO2の剥離ではなく、Mn(III)酸化物への不動態化が容量劣化の主因であることを解明
- MnO2質量基準でエネルギー密度909 Wh kg–1、パワー密度364 W kg–1を達成
研究の概要
山口大学大学院創成科学研究科の中山 雅晴教授らの研究グループと大阪大学産業科学研究所の片山 祐准教授らの研究グループは、立命館大学SRセンターの入澤 明典准教授らの研究グループ、ファインセラミックセンター(JFCC)の桑原 彰秀主席研究員らの研究グループと共同で、二酸化マンガンの析出/溶解反応に基づく2電子移動によって可逆的に動作する水系亜鉛-マンガン二次電池を開発しました。今回の技術は、弱酸性水溶液中にバッファーとFe3+イオンを添加することで、従来は非可逆であったMnO2の析出/溶解反応を完全可逆化できる点に特徴があります。電解液中の Fe3+は充電時に析出する負電荷をもつMnO2マトリックス内に取り込まれます。放電過程はMnO2からMn2+への還元溶解によって進行しますが、Fe3+未添加の場合は、プロトンの供給不足によるMnO2からMn(III)酸化物への不動態化により放電が停止します。ところが、Fe3+を添加した系では還元生成したFe2+によってMn(III)酸化物が化学的に還元され、自身は再酸化されることで、MnO2の完全溶解を仲介します。このメディエーションサイクルによって、亜鉛-マンガン電池の二次電池化に成功しました。
以上は、国立研究開発法人新エネルギー・産業総合開発機構(NEDO)の委託事業(JPNP21006)の成果であり、2025年10月3日にアメリカ化学会誌「ACS Applied Energy Materials」にオンライン版で公開され、Supplementary Coverに選定されました。
 掲載されたSupplementary Cover Art.
掲載されたSupplementary Cover Art.
研究の背景
世界的なエネルギー転換が進む中、再生可能エネルギーの導入拡大と電気自動車(EV)の普及により、蓄電池需要はかつてない速さで拡大しています。国際エネルギー機関(IEA)の試算では、2030年までに世界で数テラワット時規模の蓄電容量が必要とされ、その中で大きな割合を占めると予測されているのが、系統電力に直結する定置型大規模蓄電システムです。
リチウムイオン電池は高いエネルギー密度を誇り、携帯機器やEV用途においては大きな役割を果たしてきました。しかし、定置型用途にそのまま拡張するには問題があります。第一に、有機電解液を使用するために発火や熱暴走といった安全性リスクを内包しており、大型システムでは無視できないリスクとなります。第二に、リチウム、コバルト、ニッケルといった主要元素は地理的に偏在し、供給リスクを抱えています。このため、次世代の定置用電池には、安全性、資源持続性、低コストが強く求められています。この要請に応える有力候補の一つが水系二次電池です。水系電解液は不燃性であり、大型化しても安全に使用できる他、環境適合性やコストでも利点があります。その中でも、亜鉛(Zn)、マンガン(Mn)、鉄(Fe)は地殻存在量が豊富で、資源が特定地域に偏在せず、安定供給が可能な元素です。実際、亜鉛-マンガン一次電池※用語1は120年以上の歴史をもち、家庭や産業用途で広く使用されてきました。この一次電池を二次電池化できれば、理想的な蓄電システムとなる可能性があります。しかし、Zn-MnO2の二次電池化には、従来いくつかのアプローチが試みられてきましたが、それぞれに限界がありました。
従来研究の限界
1.強アルカリ型
・MnO2⇔Mn(OH)2間の2電子移動を利用するため理論容量※用語2が大きい(617mAh g–1)。
・固相の構造変化を伴うため、可逆性が低く、長期安定動作が困難。
2.弱酸性条件でのインサーション型
・MnO2をホストとし、Zn2+やH+が出入りする方式。
・可逆性は良好だが、1電子反応のため理論容量が小さい(308mAh g–1)。
3.強酸性水溶液中での析出/完全溶解型
・MnO2⇔Mn2+間の2電子移動を利用するため理論容量が大きい(617mAh g–1)。
・腐食の問題。導通を失ったMnO2が溶け残るため析出量を増やせない、結果として面積比容量が小さい。
今回の研究で実現したこと
- 集電体にカーボンフェルト※用語3を使用。MnO2の析出量(=面積比容量※用語4)を大幅に増大。
- 弱酸性条件を基盤とし、バッファーとFe3+レドックスメディエーター※用語5を導入することで、MnO2の析出/溶解を2電子反応でありながら完全可逆にすることに成功(図1)。
- 電気化学水晶振動子マイクロバランス(EQCM) ※用語6により、Fe3+が存在する場合、充放電過程での質量変化が完全可逆であることを実証(図2)。
- 放射光X線分析(立命館大学SRセンター)により、強酸性条件下で言われてきた“dead MnO2”の生成ではなく、Mn(III)酸化物への不動態化※用語7が非可逆性の要因であることを解明(図3)。
- Zn箔を負極、カーボンフェルトを正極に組み込んだフルセル試験において、面積比容量5 mAh cm–2でクーロン効率90%以上を達成(図4)。そのときのMnO2質量基準のエネルギー密度※用語8は909 Wh kg–1、パワー密度※用語9は364 W kg–1。
- Fe3+/Fe2+メディエーションサイクルを組み込んだ、弱酸性条件下でのMnO2析出/溶解の充放電メカニズムを提案(図5)。
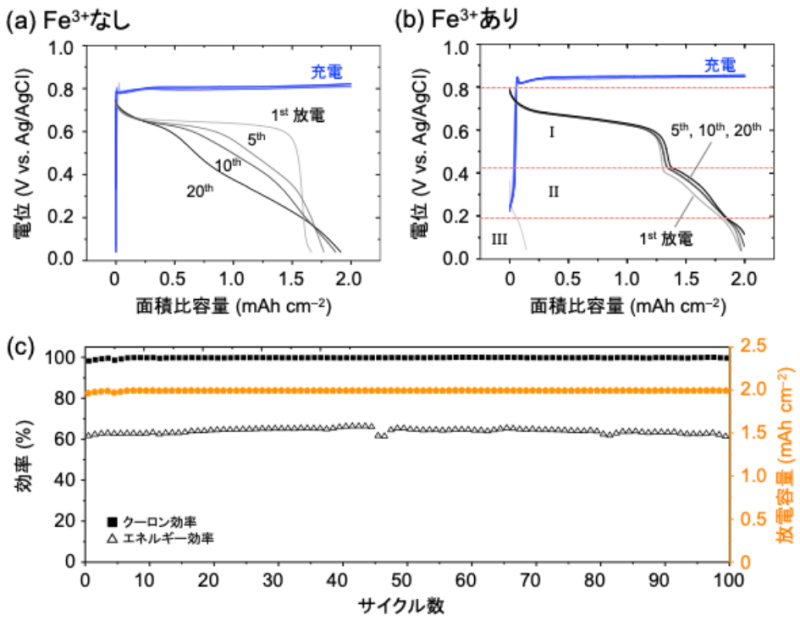 図1.Fe3+非存在下(a)および存在下(b)での定電流充放電曲線と100サイクル中のクーロン効率、エネルギー効率、面積基準の放電容量のプロット(c).
図1.Fe3+非存在下(a)および存在下(b)での定電流充放電曲線と100サイクル中のクーロン効率、エネルギー効率、面積基準の放電容量のプロット(c).
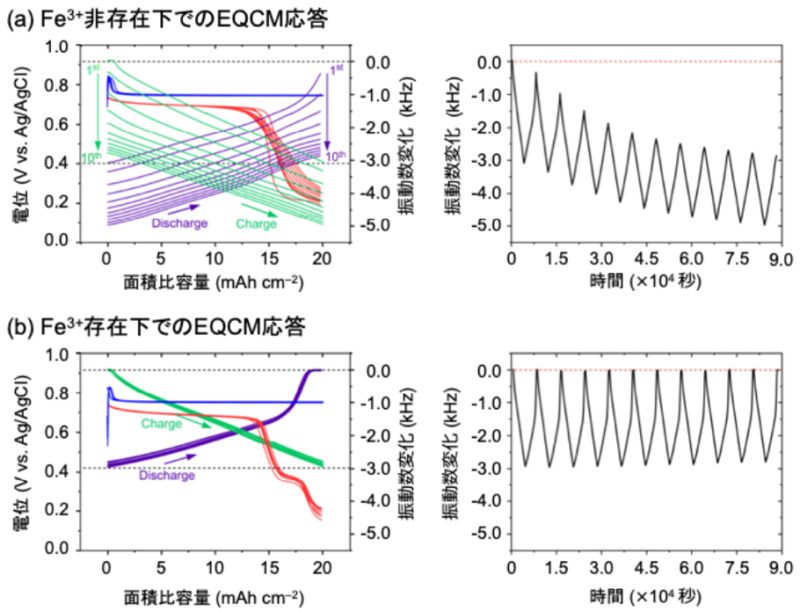 図2.Fe3+非存在下(a)および存在下(b)での定電流充放電曲線とEQCM応答.(左列)面積比容量に対する振動数変化、(右列)時間に対する振動数変化.
図2.Fe3+非存在下(a)および存在下(b)での定電流充放電曲線とEQCM応答.(左列)面積比容量に対する振動数変化、(右列)時間に対する振動数変化.
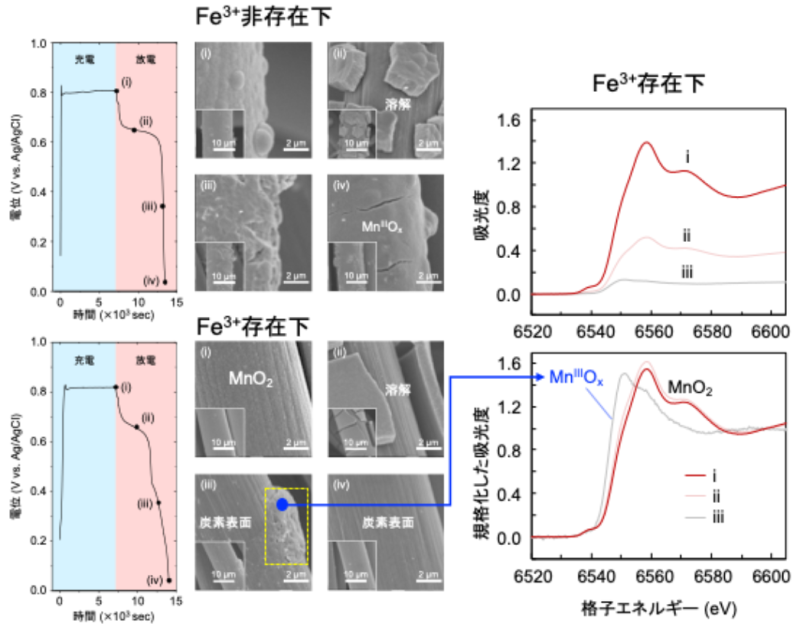
図3.Fe3+非存在下での放電過程においてポイント(i)〜(iii)で停止したときのカーボン表面のSEM像とX線吸収スペルクトル(上図はサンプル質量で、下図は6558.6 eVの強度で規格化).
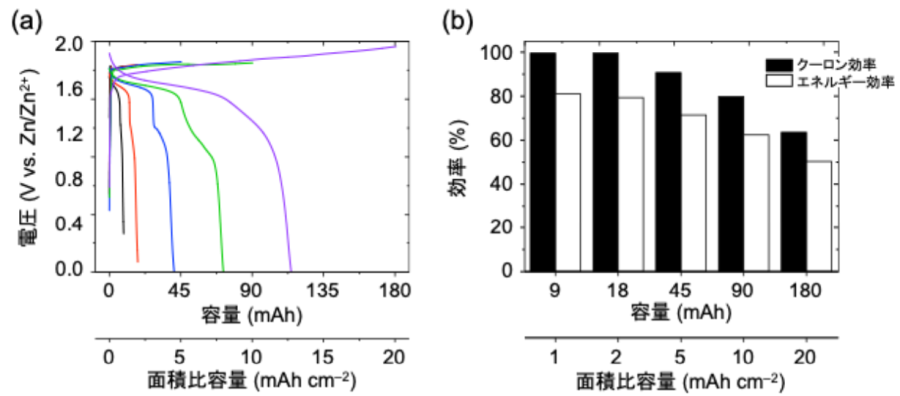
図4.Zn–カーボンフェルトフルセル([Fe3+]=1mM)において充電容量を変化させたときの放電挙動(a)とそのときのクーロン効率およびエネルギー効率(b).電解液:Mn2+ + Zn2+ + 酢酸バッファー + Fe3+.
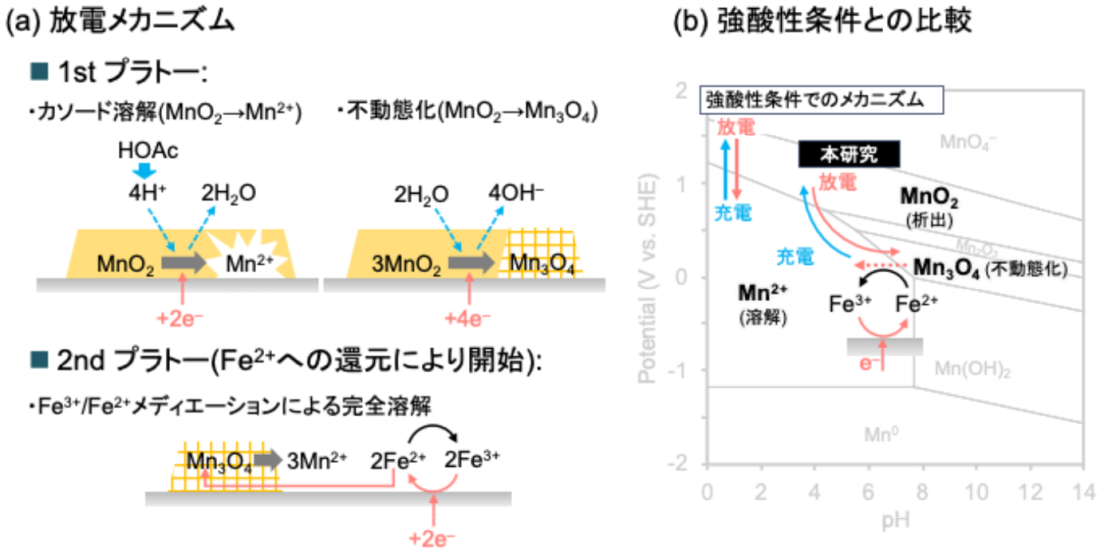 図5.放電メカニズム(a)と強酸性条件との比較(b).
図5.放電メカニズム(a)と強酸性条件との比較(b).
今後の展望
今回開発した亜鉛-マンガン二次電池は、資源的に豊富で持続可能、かつ安全で安価な材料(Zn、Mn、Fe)に基づく新しい水系電池です。長年の問題であったMnO2の低い導電性に起因する非可逆性を克服したことにより、次世代蓄電システムとして現実的な道が開かれました。
用語解説
-
※1 亜鉛-マンガン一次電池
亜鉛-マンガン一次電池は、最も広く利用されている乾電池の一種であり、アルカリ乾電池やマンガン乾電池の正式名称である。負極に亜鉛、正極に二酸化マンガンを用い、電解質には塩化アンモニウムや水酸化カリウムが使用される。放電時には亜鉛が酸化し、二酸化マンガンが還元されることで電気エネルギーが得られる。安価で安全性が高いため、懐中電灯、リモコン、時計、おもちゃなど幅広い用途に用いられている。充電して繰り返し使用できる二次電池とは異なり、一次電池は基本的に使い切りで廃棄・リサイクルされる。 -
※2 理論容量
理論容量とは、電池材料が理論上放電反応により取り出すことができる最大の電気量を指す。各活物質の化学反応式と電子の授受数、分子量から計算される値であり、単位は一般にmAhg-1で表される。 -
※3 カーボンフェルト
カーボンフェルトは、炭素繊維を三次元的に絡み合わせて形成した多孔質シート状材料である。高い電気伝導性と化学的安定性、さらに大きな比表面積を有することから、電池や電解セルの集電体として広く用いられている。特に、二酸化マンガンなどの活物質を電極表面に析出させる水系電池やレドックスフロー電池においては、反応面積を拡大し、電極反応を効率化する役割を果たす。また、機械的柔軟性にも優れ、触媒層や吸着材の担体としても利用される。 -
※4 面積比容量
面積比容量とは、電極の単位面積あたりに蓄えられる電気量を示す指標であり、単位はmAh cm–2で表される。とくに二酸化マンガン(MnO2)の析出/溶解反応を利用する水系電池においては、充電時に電極表面へ析出するMnO2の量が多いほど面積比容量は大きくなる。すなわち、同じ材料でも、集電体の比表面積や反応場の設計により、MnO2の析出量を増大させることで面積比容量を高めることができる。実使用を想定した場合、限られた電極面積内にできるだけ多くの活物質を安定に析出・利用できることが、高性能化の鍵となる。 -
※5 レドックスメディエーター
レドックスメディエーターとは、電極と活物質との間で電子の受け渡しを仲介する化学種である。自身が可逆的に酸化・還元反応を行うことで電子を運び、電極反応を間接的に促進する役割を果たす。例えば、今回のMnO2析出/溶解反応で言えば、電解液中に溶解したFe3+/Fe2+のようなレドックスメディエーターが電子伝達を仲介することで、MnO2からMn2+への溶解を促進する。これにより、電極反応の過電圧を低減し、容量やエネルギー効率を高めることが可能になる。直接の固体表面反応に依存する場合と比べて、反応の進行が均一かつ効率的になる点が特徴である。 -
※6 電気化学水晶振動子マイクロバランス(EQCM)
電気化学水晶振動子マイクロバランス(EQCM)は、水晶振動子の共振周波数変化を利用して、電極表面での質量変化をナノグラム単位で測定できる分析手法である。電気化学測定と同時に行うことが可能であり、電極反応に伴う析出・溶解やイオン吸脱着の過程をリアルタイムで追跡できる点が特徴である。例えば、MnO2析出/溶解型の電池反応を調べる際には、電極表面に析出するMnO2の量や、溶解による質量減少を直接モニターすることができ、反応機構の解明に有効である。 -
※7 不動態化
不動態化とは、金属や酸化物の表面に化学的に安定で電気的に不活性な層が形成されることにより、電極反応が進行しなくなる現象を指す。電極表面が不動態化すると、電子やイオンの移動が阻害され、電気化学反応の効率が低下する。例えば、MnO2を正極として用いる場合、充放電の過程でMnO2が電気化学的に不活性なMn3O4へと変化すると、反応に寄与する活物質が減少し、容量やサイクル寿命の低下を招く。このように、不動態化は電池性能を制限する要因の一つである。 -
※8 エネルギー密度
エネルギー密度とは、電池が単位質量または単位体積あたりに蓄えられるエネルギー量を指す指標である。一般にWh kg–1やWh L–1で表され、電池の小型化や軽量化の目安として重要である。エネルギー密度の値は、基準とする質量や体積の範囲によって変化する。例えば、正極活物質のみの質量を基準にすれば高い値となるが、負極や電解液、セパレーター、集電体を含めたセル全体の質量を基準にすると低い値となる。したがって、エネルギー密度を比較する際には、どのレベル(材料、電極、セル、モジュール)を基準としているかを明示する必要がある。 -
※9 パワー密度
パワー密度とは、電池が単位質量または単位体積あたりに瞬時に取り出すことのできる出力(電力)を示す指標である。一般にW kg–1やW L–1で表され、エネルギー密度が「どれだけ長く使えるか」を示すのに対し、パワー密度は「どれだけ速くエネルギーを出せるか」を示す。値は基準とする質量や体積に依存し、活物質のみを基準にする場合と、セル全体を基準にする場合で異なる。
論文情報
- 雑誌名:ACS Applied Energy Materials
- 論文名:An Fe3+-Responsive MnO2/Mn2+ Cathode for Zinc-Ion Batteries: Fe3+ Incorporated into MnO2 during Charging Accelerates its Dissolution during Discharging
- 執筆者名:Koki Obuchi, Jin Kitamura, Misaki Ando, Kota Kamo, Kota Nakamura, Eiki Mukayabu, Tomohiko Utsunomiya, Yasuyuki Kondo, Yuki Sasaki, Kaname Yoshida, Yuki Yamada, Akinori Irizawa, Akihide Kuwabara, Wataru Yoshida, Kiyotaka Asakura, Yu Katayama, Masaharu Nakayama*
- 掲載日:2025年10月3日
- 掲載URL:https://pubs.acs.org/doi/full/10.1021/acsaem.5c01923
- DOI:10.1021/acsaem.5c01923
研究助成
国立研究開発法人新エネルギー・産業総合開発機構(NEDO)の委託事業(JPNP21006)
お問い合わせ
<本研究に関するお問い合わせ先>
- 山口大学大学院創成科学研究科 教授 中山 雅晴
Tel:0836-85-9223
E-mail:nkymm@(アドレス@以下→yamaguchi-u.ac.jp) - 大阪大学産業科学研究所 准教授 片山 祐
Tel:06-6879-8522
E-mail:yuktym@(アドレス@以下→sanken.osaka-u.ac.jp)
<報道に関するお問い合わせ先>
-
山口大学総務企画部総務課広報室
Tel:083-933-5007
E-mail:sh011@(アドレス@以下→yamaguchi-u.ac.jp) -
大阪大学産業科学研究所広報室
Tel:06-6879-8524
E-mail:press@(アドレス@以下→sanken.osaka-u.ac.jp) -
立命館大学総合企画部広報課
Tel:075-813-8300
E-mail:r-koho@(アドレス@以下→st.ritsumei.ac.jp) -
ファインセラミックスセンター
Tel:052-871-3500
E-mail:ressup@(アドレス@以下→jfcc.or.jp)

