CRISPR-Cas3でヒトT細胞遺伝子破壊に成功 ―次世代CAR-T細胞治療への応用に期待―
発表のポイント
- CRISPR-Cas3システムを用いて、ヒトT細胞の遺伝子を高効率に破壊するゲノム編集技術を開発しました。
- 従来広く利用されているCRISPR-Cas9がDNAを一カ所で切断するのに対し、Cas3はDNAを連続的に分解する特徴を持ち、大規模DNA欠失による確実な遺伝子ノックアウトを実現しました。
- 免疫関連遺伝子を破壊したT細胞より作製したCAR-T細胞が腫瘍細胞を殺傷できることを確認したことから、本技術は、同種移植型CAR-T細胞など次世代の細胞治療技術の基盤になる可能性があります。
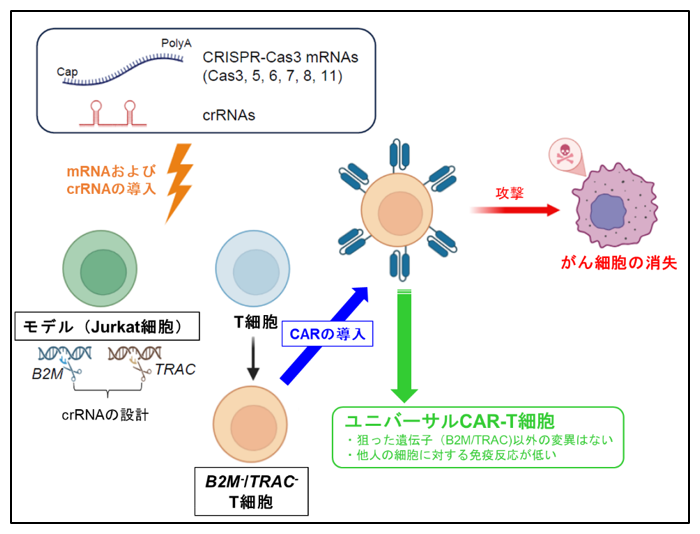
CRISPR-Cas3によるユニバーサルCAR-T細胞作製の概要
概要
東京大学医科学研究所先進動物ゲノム研究分野の真下知士教授、藤井智明研究員(研究当時)、山口大学大学院医学系研究科免疫学講座の玉田耕治教授、理化学研究所放射光科学研究センターの竹下浩平研究員らの研究グループは、CRISPR-Cas3システム(注1)を用いてヒトT細胞(注2)の遺伝子を効率的に破壊するゲノム編集技術(注3)を開発しました。
ゲノム編集技術の1つであるCRISPR技術(注4)は生命科学研究や医療分野で利用されています。中でも広く用いられているCRISPR-Cas9はDNAを一カ所で切断する仕組みですが、細胞の修復過程によって小さな変異が導入されるだけで遺伝子機能が完全に失われない場合があります。また、標的とは異なるDNA配列を誤って切断してしまう可能性(オフターゲット効果:注5)があることも課題とされています。
本研究では、真下教授らのグループによって真核細胞でのゲノム編集活性が報告されている、Type I CRISPRシステムに属するCRISPR-Cas3に着目しました。構成因子の1つであるCas3は標的DNAを認識した後、DNAを連続的に分解する酵素であり、この特徴により標的遺伝子周辺に広範囲のDNA欠失を誘導することができます。この特性を利用し、CRISPR-Cas3 mRNA(注6)をヒトT細胞に導入し、免疫関連遺伝子であるTRAC(注7)およびB2M(注8)遺伝子を標的としてゲノム編集を行いました。その結果、これらの遺伝子を、オフターゲット効果を認めずに高効率に破壊することに成功しました。さらに、これらの遺伝子編集T細胞からCAR-T細胞(注9)を作製して機能を評価し、腫瘍細胞に対する殺傷活性が維持されていることを確認しました。
本研究成果は、ヒトT細胞の遺伝子を高効率に破壊できる新しいゲノム編集技術として、遺伝子編集を利用した次世代の細胞治療技術の開発に貢献することが期待されます。特に、免疫関連遺伝子を改変したT細胞は、同種移植型CAR-T細胞などの新しいがん免疫療法の開発において重要な役割を果たす可能性があります。
本研究成果は2026年4月21日午前0時(UTC)(日本時間4月21日午前9時)に、英国科学雑誌「NAR cancer」オンライン版で公開されました。
発表内容
〈研究の背景〉
近年、CRISPR-Cas9をはじめとするゲノム編集技術は急速に発展しており、疾患の原因遺伝子を改変することで新たな治療法を開発する研究が進んでいます。特に、患者の免疫細胞を遺伝子改変してがん細胞を攻撃させるCAR-T細胞療法は、白血病やリンパ腫などの血液がんに対して高い治療効果を示すことが知られています。一方で、現在のCAR-T細胞療法は患者自身の細胞を用いて作製する必要があるため、製造に時間とコストがかかるという課題があります。この問題を解決するため、健康なドナー由来のT細胞を遺伝子改変して作製する「ユニバーサルCAR-T細胞(注10)」の開発が進められています。しかしながら、他人由来のT細胞をそのまま移植すると、T細胞受容体(注11)による免疫反応によって移植片対宿主病(GVHD)(注12)が引き起こされる可能性があります。また、患者側の免疫系によって細胞が排除される免疫拒絶の問題もあります。そのため、ユニバーサルCAR-T細胞を実現するためには、T細胞受容体遺伝子やHLA関連遺伝子などを効率的かつ安全に破壊するゲノム編集技術が必要とされています。
これまで広く利用されてきたCRISPR-Cas9システムは強力な遺伝子編集ツールですが、標的DNA配列と類似した配列を誤って切断するオフターゲット効果や、DNA二本鎖切断に伴う染色体転座などのゲノム不安定性が生じる可能性が指摘されており、臨床応用に向けては安全性の検証が求められています。一方、CRISPRシステムの一種であるCas3は、標的DNAを認識した後、その位置からDNAを一方向に連続的に分解していくプロセッシブ分解(processive degradation)を導くという特徴を持つCRISPR酵素です。この作用により、Cas9のように特定の位置を切断するのとは異なるメカニズムで遺伝子破壊を引き起こします。また、Cas3を利用するCRISPRシステムでは、標的配列を認識するガイドRNA(crRNA、注13)がCas9よりも長い配列を持つため、標的DNAをより厳密に識別できることが実証されています。こうした特徴から、Cas3は高い特異性を持つ新しいゲノム編集ツールとして注目されています。しかし、ヒトの免疫細胞におけるCas3の応用例はまだ限られており、その有効性や安全性については十分に検証されていませんでした。
〈研究の内容〉
本研究では、CRISPR-Cas3システムを用いることで、ヒトT細胞において複数の免疫関連遺伝子を効率的に破壊し、CAR-T細胞療法への応用が可能であることを示しました。まず、ユニバーサルCAR-T細胞の作製において重要とされる遺伝子として、T細胞受容体を構成するTRAC遺伝子と、HLAクラスI分子の発現に関与するB2M遺伝子に着目しました。これらの遺伝子を破壊することで、移植片対宿主病(GVHD)の原因となるT細胞受容体の発現を抑制するとともに、患者の免疫系による細胞排除を回避できる可能性があります。Cas3複合体と標的配列を認識するcrRNAをヒトT細胞に導入し、TRACおよびB2M遺伝子領域に対してゲノム編集を誘導しました。その結果、Cas3によるDNA分解が標的領域において効率的に誘導され、TRAC遺伝子およびB2M遺伝子の機能を破壊したT細胞の作製に成功しました(編集効率:それぞれ平均34.7%、45.0%)。さらに、両遺伝子を破壊した細胞において、高い生存率が維持されていることを確認しました(図1)。
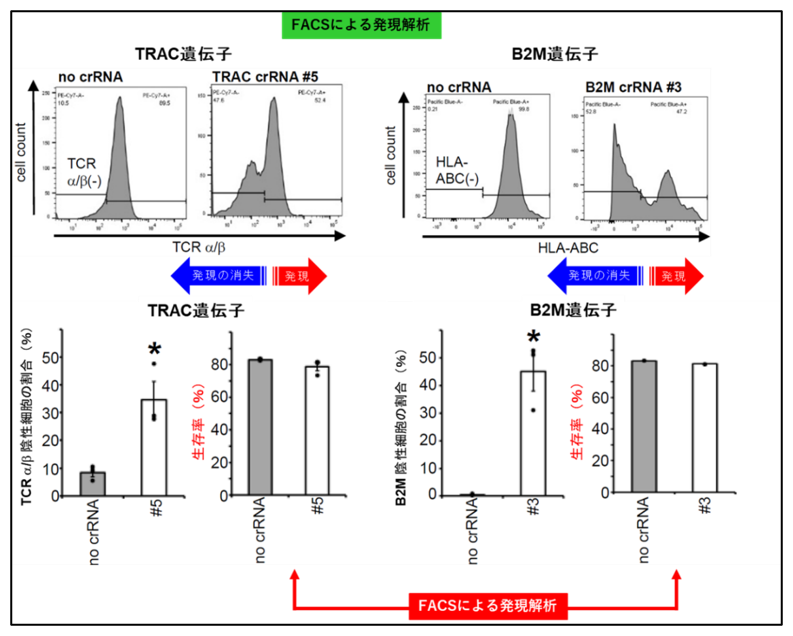
図1:CRISPR-Cas3システムを用いたT細胞のTRAC遺伝子およびB2M遺伝子のゲノム編集
さらに、作製した改変T細胞のゲノム構造を解析したところ、Cas3による編集は標的領域において、顕著なオフターゲット効果は検出されず、極めて高い標的特異性を持つことを示しました。また、広い範囲のDNA欠失を伴う遺伝子破壊を引き起こすことを確認しました(図2)。
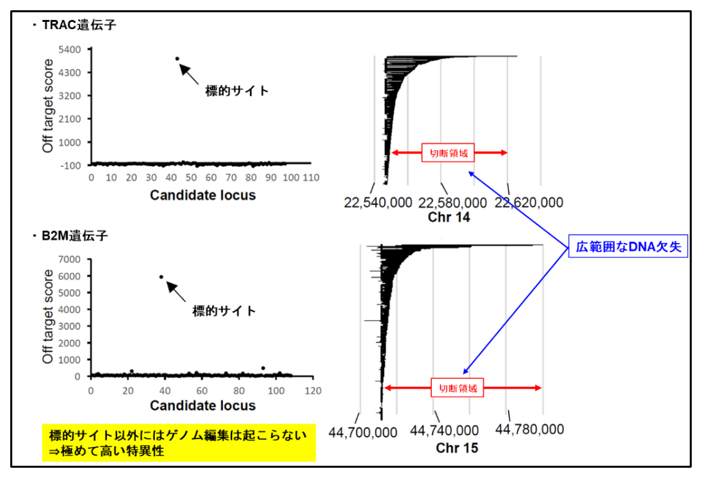
図2:CRISPR-Cas3を用いたゲノム編集により作製したT細胞のゲノム解析
これらの遺伝子編集T細胞からCAR-T細胞を作製し、標的とする腫瘍細胞に対する殺傷活性を評価したところ、遺伝子編集を行っていないCAR-T細胞と同様に高い抗腫瘍活性を示すことを確認しました(図3)。これらの結果は、CRISPR-Cas3によるゲノム編集がヒトT細胞においても有効に機能し、免疫細胞療法に利用可能なCAR-T細胞の作製に応用できる可能性を示しています。
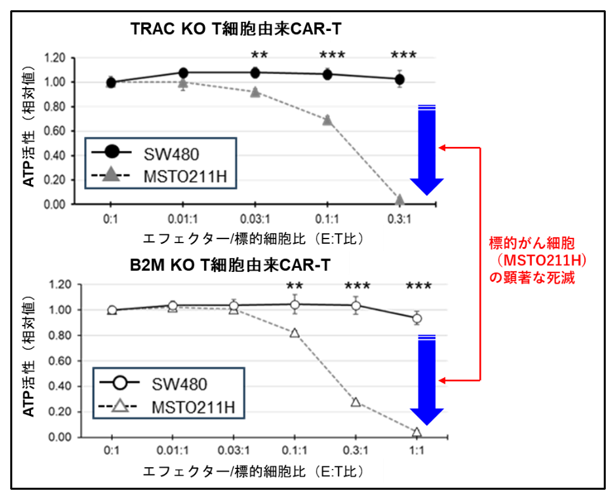
図3:CRISPR-Cas3によりゲノム編集を行ったT細胞より作成したCAR-T細胞の活性
〈今後の展望〉
本研究で開発したCRISPR-Cas3システムによるヒトT細胞のゲノム編集技術は、遺伝子機能を確実に失わせることが求められる細胞治療研究において重要な意義を持ちます。また、TRACやB2M遺伝子など免疫機能に関わる遺伝子を破壊したT細胞は、同種移植型(オフ・ザ・シェルフ型)CAR-T細胞など次世代の細胞治療技術の開発に貢献することが期待されます。さらに、遺伝子編集T細胞から作製したCAR-T細胞が腫瘍細胞に対して高い殺傷活性を維持することも判明し、本技術ががん免疫療法の新しい基盤技術となる可能性が示されました。CRISPR-Cas3は従来広く用いられてきたCRISPR-Cas9とは異なるタイプのCRISPR技術であり、今後のゲノム編集研究や細胞治療の発展に新たな可能性をもたらすことが期待されます。
今後は、本技術の安全性や有効性をさらに検証することで、遺伝子編集を利用した新しい細胞治療の実現につながることが期待されます。
発表者・研究者情報
- 山口大学大学院医学系研究科 免疫学講座
・玉田 耕治 教授(細胞デザイン医科学研究所 所長)
(兼:東京大学医科学研究所 附属遺伝子・細胞治療センター 委嘱教授)
・佐古田 幸美 准教授(細胞デザイン医科学研究所) - 東京大学医科学研究所 附属実験動物研究施設 先進動物ゲノム研究分野
・真下 知士 教授
・吉見 一人 准教授
・藤井 智明 特任助教:研究当時
・渡辺 祥司 共同研究員
・横山 一剛 共同研究員:研究当時
・飯田 龍哉 東京大学大学院新領域創成科学研究科 博士課程
・大保 翼 東京大学大学院新領域創成科学研究科 修士課程 - 理化学研究所 放射光科学研究センター 生物系ビームライン基盤グループ
・竹下 浩平 研究員
論文情報
- 雑誌名:NAR Cancer
- 題名:Efficient gene disruption with CRISPR-Cas3 in human T cells
- 著者名:Tomoaki Fujii, Yukimi Sakoda, Kazuto Yoshimi, Kohei Takeshita, Shoji Watanabe, Ryuya Iida, Tsubasa Obo, Kazumasa Yokoyama, Koji Tamada, and Tomoji Mashimo*(*責任著者)
- DOI:10.1093/narcan/zcag009
- URL:https://academic.oup.com/narcancer/article-lookup/doi/10.1093/narcan/zcag009
研究助成
本研究は、日本医療研究開発機構(AMED)先端的バイオ創薬等基盤技術開発事業「新規ゲノム編集技術を用いた次世代CAR-T細胞療法の開発」、再生医療実現拠点ネットワークプログラム「ムコリピドーシス(ICD)を対象としたCRISPR-Cas3系ゲノム編集技術により作製した胎児付属物由来造血幹細胞製剤のPOC取得」、再生・細胞医療・遺伝子治療実現加速化プログラム「CRISPR-Cas3 mRNA-LNPモダリティによる安全なin vivoゲノム編集治療基盤の構築」、再生・細胞医療・遺伝子治療実現加速化プログラム「造血幹細胞増幅技術を基盤とした改変造血・免疫細胞の創出と応用」の支援により実施されました。
用語解説
- (注1)CRISPR-Cas3システム:
細菌由来の免疫機構を応用したゲノム編集技術の一種で標的DNAを広範囲に分解する特徴を持つ。 - (注2)T細胞:
免疫反応を担うリンパ球の一種。 - (注3)ゲノム編集技術:
DNA配列を人為的に改変する技術。 - (注4)CRISPR技術:
特定のDNA配列を狙って改変できる遺伝子操作技術。 - (注5)オフターゲット効果:
標的以外のDNA配列が誤って編集される現象。 - (注6)mRNA:
タンパク質の設計図となる分子。 - (注7)TRAC遺伝子:
T細胞受容体の構成に関わる遺伝子。 - (注8)B2M遺伝子:
HLAクラスI分子の発現に関与する遺伝子。 - (注9)CAR-T細胞:
遺伝子改変によりがん細胞を攻撃できるようにしたT細胞。 - (注10)ユニバーサルCAR-T細胞:
汎用的に使用可能なCAR-T細胞。 - (注11)T細胞受容体:
T細胞が抗原を認識するための分子。 - (注12)移植片対宿主病(GVHD):
移植された免疫細胞が患者の体を攻撃する病態。 - (注13)ガイドRNA(crRNA):
標的とするDNA配列を認識し、CRISPR酵素を目的の位置へ導くRNA分子。
お問い合わせ先
- 山口大学大学院医学系研究科 免疫学講座
細胞デザイン医科学研究所
教授 玉田 耕治(たまだ こうじ)
E-mail:immunol@(アドレス@以下→yamaguchi-u.ac.jp) - 東京大学医科学研究所 附属実験動物研究施設 先進動物ゲノム研究分野
教授 真下 知士(ましも ともじ)
Tel:03-6409-2228
E-mail:mashimo@(アドレス@以下→ims.u-tokyo.ac.jp)
- 山口大学医学部総務課 広報・国際係
Tel:0836-22-2009
E-mail:me268@(アドレス@以下→yamaguchi-u.ac.jp) - 東京大学医科学研究所 プロジェクトコーディネーター室(広報)
Tel:090-9832-9760
E-mail:koho@(アドレス@以下→ims.u-tokyo.ac.jp) - 理化学研究所 広報部 報道担当
Tel:050-3495-0247
E-mail:ex-press@(アドレス@以下→ml.riken.jp)

