非光合成生物が光合成能力を獲得する仕組みの初期条件を発見 -ミドリゾウリムシとクロレラの細胞内共生で、宿主ミトコンドリアとクロレラ包膜間の強固な結合を初めて証明-
発表のポイント
- ミドリゾウリムシから、共生クロレラ・共生藻包膜(PV膜※1)・ミトコンドリア※2からなる機能ユニットの単離技術の確立に成功
- PV膜とミトコンドリア膜を、蛍光標識脂質(BODIPY FL C5-ceramide※3)により同時に可視化する手法を開発
- PV膜と宿主ミトコンドリア外膜の結合が、細胞破壊や遠心処理後も維持される「構造的に安定した強固な結合」であることを初めて証明
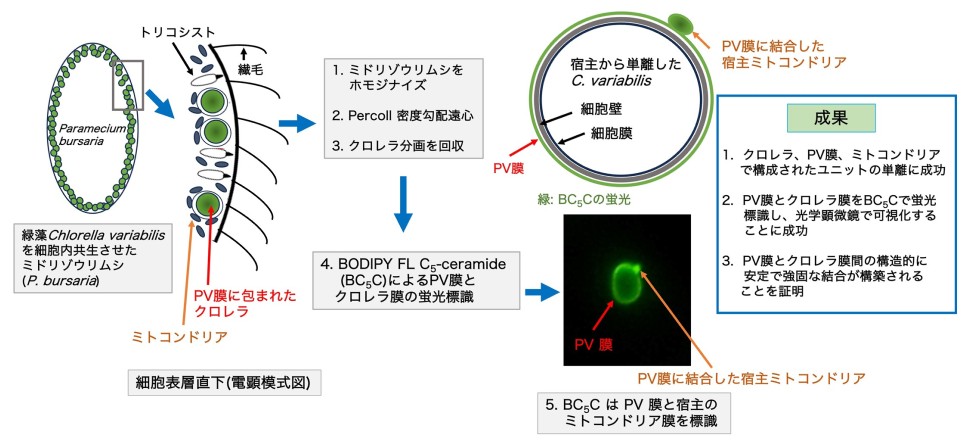
図1.実験の概要
概要
光合成※4能力を持たない生物が、藻類やその葉緑体※5を細胞内に取り込んで光合成産物(糖や酸素)を利用する能力を獲得する現象は、「光合成細胞内共生」と呼ばれます。これは非光合成生物にとって極めて有利な生存戦略であり、生物進化の重要な過程の一つです。
山口大学大学研究推進機構「中高温微生物研究センター」および福島大学環境放射能研究所の客員研究員である藤島政博 山口大学名誉教授と、山口大学理学部卒業生の西山翔氏は、ミドリゾウリムシ(Paramecium bursaria)とその細胞内共生クロレラ(Chlorella variabilis)を用い、共生藻を包む宿主由来の膜(PV膜)と宿主ミトコンドリア外膜との間に、構造的に安定した強固な結合が形成されていることを明らかにしました(図1)。
研究背景
繊毛虫のミドリゾウリムシは光合成細胞内共生の成立機構の解明に適したモデル生物です。ミドリゾウリムシの細胞長は約100 μmで、細胞内に300〜500個のクロレラを共生させているため緑色をしています(図2)。宿主はクロレラを細胞内共生させることによって、飢餓、高温、紫外線、高塩濃度に対する耐性を獲得し、生存に有利になります(引用論文1)。
外液から宿主の食胞に取り込まれたクロレラは、食胞膜の出芽によって個別に宿主細胞質に脱出し、その後、クロレラを包む膜がライソソーム融合阻止能力を持つPV膜に分化し、PV膜に包まれたクロレラが宿主の細胞表層直下に移動してそこに安定して局在することが明らかにされています(引用論文2)。PV膜は薄い単位膜※6でクロレラの細胞壁との間隔も狭いため電子顕微鏡でしか見ることができない膜です。電子顕微鏡観察ではPV膜が宿主細胞表層直下に高密度で存在するミトコンドリアの外膜と接触している像が観察されています(引用論文3, 4)。また、細胞内共生能力を持たないクロレラ種は、食胞からの脱出はできますが細胞表層直下に局在することができずに細胞内共生に失敗します(引用論文2)。遺伝的にクロレラを細胞内共生させることができない宿主は、細胞内共生能力をもつクロレラと混合しても食胞脱出後に宿主細胞表層直下に局在させることができず、宿主の細胞分裂時に娘細胞への分配に失敗して白色細胞に戻ることが知られています(引用論文5)。さらに、緑色細胞に強い遠心をかけると、クロレラが細胞表層から剥がれて宿主細胞後端に堆積し、遠心を止めると同時に原形質流動によって浮遊したクロレラが15分以内に細胞表層直下に再び局在化することが明らかにされています(引用論文6)。
これらの現象は、宿主細胞表層直下へのクロレラの局在が細胞内共生成立の必須現象であることを示していますが、PV膜とミトコンドリア外膜との接触がどれほど強く安定的なものかは未解明でした。この2種類の単位膜の接触が構造的に安定した強い結合であることを確認し、その必要性を解明する必要があります。ここからこの研究テーマを飛躍的に進展させる突破口が見えそうです。光合成細胞内共生を行う他の生物でも共生藻とミトコンドリアが同じ領域に近接して局在する現象が確認できることがそれを示しています。
研究の成果
本研究は、電子顕微鏡で観察されていたミドリゾウリムシのPV膜と宿主のミトコンドリア外膜との接触が、構造的に安定した強固な結合なのかどうかを明らかにする目的で行われました。
最初に、ミトコンドリア特異的モノクローナル抗体※7とDNA結合蛍光色素DAPI※8を用いて、宿主細胞内でのミトコンドリアと共生クロレラの存在場所を調べました。細胞表層直下にミトコンドリアが高密度で存在し、そのミトコンドリアがクロレラを取り囲んでいるように配置していることを確認しました(図3)。
次に、宿主細胞をテフロンホモジナイザーで破壊し、Percoll※9不連続密度勾配遠心で、PV膜に包まれたクロレラとミトコンドリアを共沈させて回収する技術の開発を試みました。ミトコンドリアは前述のモノクローナル抗体とDAPI染色で識別しました。その結果、クロレラにミトコンドリアが付着し、共沈したことが確認できました(図4)。
続いて、PV膜の有無とミトコンドリアの付着の関係を調べました。PV膜は緑色蛍光色素で標識した膜脂質(BODIPY FL C5-ceramide complexed to BSA、BC5C/BSA)を用いて蛍光顕微鏡で単離されたクロレラを包んでいるかどうかを確認しました。BC5C/BSAは生体膜の脂質に接近すると、BSAを解離したBC5CがBSAよりも疏水結合力が強い生体膜の脂質と結合することで生体膜を蛍光顕微鏡で可視化することが知られています。BC5Cは、単離されたクロレラの外周とそれに付着したミトコンドリアを同時に蛍光標識しました。一方、BC5Cで標識されないクロレラ(PV膜を失ったクロレラ)にはミトコンドリアの付着は観察できませんでした(図5)。従来の電子顕微鏡観察ではクロレラの細胞壁はPV膜以外の生体膜で囲まれていないことから、 BC5CはPV膜を標識し、同時にミトコンドリア膜をも標識したことを示しています。また、 BC5CはPV膜を貫通してその内側に移動しないことと、クロレラの細胞壁を標識できないことも分かりました。単離されたクロレラの約77%においてPV膜がついた状態で単離され、さらに、そのPV膜にはミトコンドリアの付着が確認されました。PV膜を欠失して単離されたクロレラ細胞壁にはミトコンドリアの付着は認められませんでした。
これらの結果は、クロレラ、PV膜、ミトコンドリアを1ユニットとして単離する技術開発に成功したことと、PV膜と宿主ミトコンドリア膜との接着が、ホモジナイズや遠心力に耐えるほどの強い結合で、クロレラを宿主細胞の表層直下に局在させる要因であることが強く示唆されました。
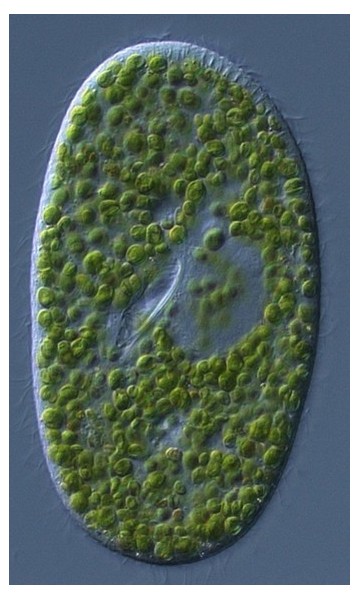 図2.ミドリゾウリムシの微分干渉顕微鏡写真
図2.ミドリゾウリムシの微分干渉顕微鏡写真
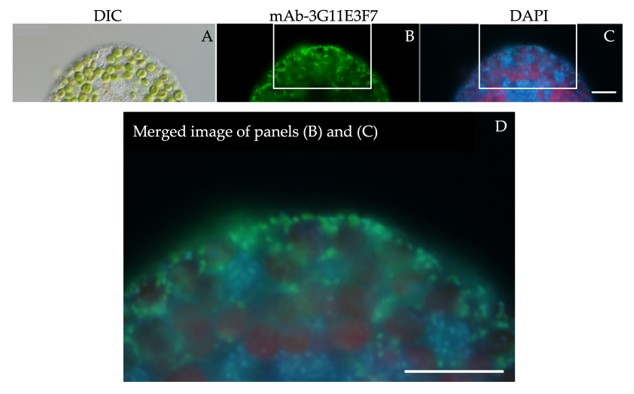 図3.抗ミトコンドリア抗体を使った間接蛍光抗体法写真とDAPI染色写真
図3.抗ミトコンドリア抗体を使った間接蛍光抗体法写真とDAPI染色写真
(A) 微分干渉顕微鏡写真、(B) 間接蛍光抗体法写真、(C) DAPI染色写真、(D) BとCの重ね合わせ写真、スケールバー: 10 μm。
ミトコンドリアがクロレラを取り囲んで配置している (B–D).
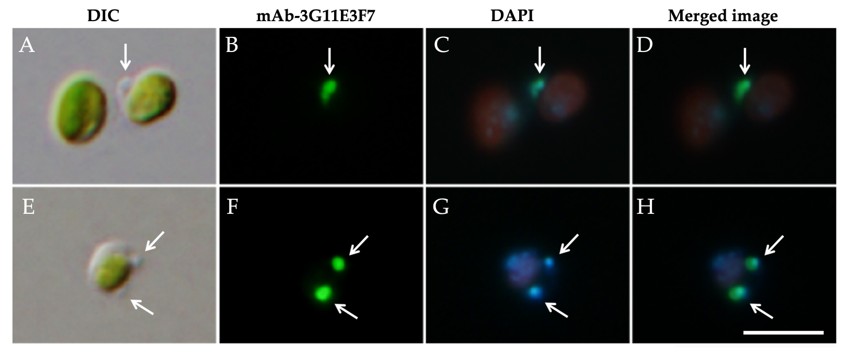 図4.宿主細胞をホモジナイズし、Percoll密度勾配遠心で単離したクロレラ分画
図4.宿主細胞をホモジナイズし、Percoll密度勾配遠心で単離したクロレラ分画
(A, E) 微分干渉顕微鏡写真、(B, F) 抗ミトコンドリア抗体を使った間接蛍光抗体法写真、(C, G) DAPI染色写真、(D, H) 重ね合わせ写真。スケールバー: 10 μm。
宿主細胞から単離されたクロレラに宿主のミトコンドリア(矢印)が結合している。
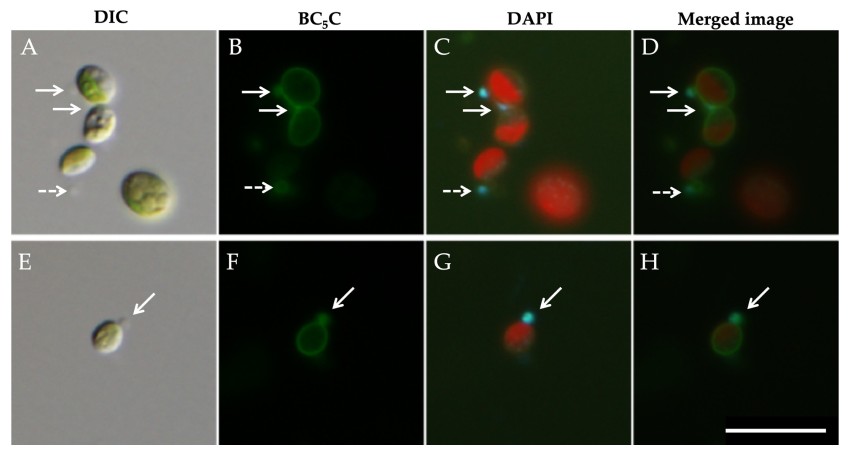 図5.細胞をホモジナイズし、Percoll密度勾配遠心で単離したクロレラ分画
図5.細胞をホモジナイズし、Percoll密度勾配遠心で単離したクロレラ分画
(A, E) 微分干渉顕微鏡写真、 (B, F) BC5C標識写真、(C, G) DAPI染色写真、(D, H) 重ね合わせ写真。
クロレラを包むPV膜とミトコンドリアがBC5Cで標識された (B, F)。
矢印:PV膜に接着しているミトコンドリア。破線矢印:PV膜に結合していないクロレラ。PV膜がBC5Cで標識されている。
(B–D, F–H) PV膜とミトコンドリアが接着している。(A, B) クロレラはPV膜を失ったクロレラには接着できない。スケールバー: 10 μm。
本研究の意義と今後の展開
光合成能力を持っていない真核生物が光合成細胞内共生によって藻類の機能を獲得する究極の進化の実現の最初の一歩が、PV膜と宿主ミトコンドリア外膜との構造的に安定した強固な接着であることが明らかになりました。強固な接着の必要性の解明と接着部位構成物質の解明、そして光合成細胞内共生における普遍性の確認、それらの情報を使用した人工的な光合成細胞内共生の誘導と有用生物の作成が今後の課題です。
用語解説
- ※1 PV膜(Perialgal vacuole膜の略称):
ミドリゾウリムシでは食胞に取り込まれたクロレラが食胞膜の出芽で食胞膜に包まれて細胞質に脱出し、その後、食胞膜由来のクロレラを包む膜がライソソーム融合阻止能力とミトコンドリア外膜との結合能力などを獲得したPV膜に分化する。PV膜に存在するタンパク質の種類はまだ未確定。同様の起源と機能を持つ共生藻包膜は多数の生物で知られている。 - ※2 ミトコンドリア:
脂質二重層でできた外膜と内膜の生体膜を持ち、酸素分子を利用してATPを合成する。内部には独自のDNAが存在する。 - ※3 BODIPY FL C5-ceramide(略称 BC5C):
蛍光色素BODIPYで標識されたセラミドで、水溶性にするためにBSAを疏水結合させて使用し、生細胞に与えると細胞膜に接近したときに、BSAが分離し、より親和性が強い脂質二重層に結合することで生体膜を緑色蛍光で可視化することができる。 - ※4 光合成:
光エネルギーを利用して無機炭素から有機化合物を合成する反応で、その過程で水が分解されて酸素が放出される。光合成は植物、藻類、光合成細菌が行い、地球上のほぼ全ての酸素は光合成に由来する。ミドリゾウリムシのクロレラはマルトースを合成している。 - ※5 葉緑体:
光合成を行う細胞小器官で、内部に独自のDNAが存在する。葉緑体は外膜(外包膜)と内膜(内包膜)の二重の生体膜で囲まれた構造をしているが、その起源によっては三重膜や四重膜のものもある。葉緑素はチラコイドと呼ばれる円盤状の小胞に収められ、光合成の初期反応はチラコイド膜で行われる。チラコイド膜上ではATP合成酵素がATPを合成する。 - ※6 単位膜(生体膜):
二重層のリン脂質にタンパク質などが埋め込まれた膜構造で、細胞膜や細胞小器官の膜に共通する基本構造の膜。 - ※7 モノクローナル抗体:
単一の抗体産生細胞をクローニングして作られた抗体で、一種類の抗原決定基を認識する抗体。 - ※8:DAPI(4‘,6-diamidino-2-phenylindoleの略称):
蛍光色素の一種で、DNAに対して強力に結合する物質で、蛍光顕微鏡観察に使用される。 - ※9 Percoll:
比重の違いを利用して密度勾配遠心で単離・精製するための親水性シリカゾル
謝辞
本研究は、日本学術振興会科学研究費基盤研究B(22370082)と文部科学省特別経費の支援を受けて行われました。
引用論文
- Kodama Y., Fujishima M. Microorganisms, 2024, 12(12), 2537. DOI: 10.3390/microorganisms12122537
- Kodama Y., Fujishima M. Protoplasma 2007, 231, 55–63. DOI: 10.1007/s00709-006-0241-8
- Kodama Y., Fujishima M. FEMS Microbiol. Lett. 2023, fnad088 DOI: 10.1093/femsle/fnad088
- Song C. et al. Sci. Rep. 2017, 7, 1221. DOI: 10.1038/s41598-017-01331-0
- Tonooka Y., Watanabe T. Invertebr.Biol. 2007, 126, 287–294. DOI: 10.1111/j.1744-7410.2007.00099.x
- Kodama Y., Fujishima M. Protist 2013, 164, 660–672. DOI: 10.1016/j.protis.2013.07.001
発表論文の情報
- 論文名:First evidence for a structurally stable adhesion between the perialgal vacuole membrane and host mitochondria in the Paramecium–Chlorella endosymbiosis
(ゾウリムシとクロレラの細胞内共生ではPV膜と宿主のミトコンドリアとの間に構造的に安定した結合が形成されることを示す初の証拠) - 著者:Masahiro Fujishima and Sho Nishiyama(藤島政博、西山翔)
- 掲載雑誌(出版社):Biomolecules(スイスMDPI)
- 掲載日:2026年4月10日18:00(日本時間)
- DOI:https://doi.org/10.3390/biom16040561
お問い合わせ先
- <研究に関すること>
山口大学 大学研究推進機構 中高温微生物研究センター環境微生物部門
客員研究員 藤島 政博(フジシマ マサヒロ)
Tel:080-3051-1471
E-mail:fujishim@(アドレス@以下→yamaguchi-u.ac.jp) - <報道に関すること>
山口大学 総務部総務課広報室
Tel:083-933-5007
E-mail:sh011@(アドレス@以下→yamaguchi-u.ac.jp)

